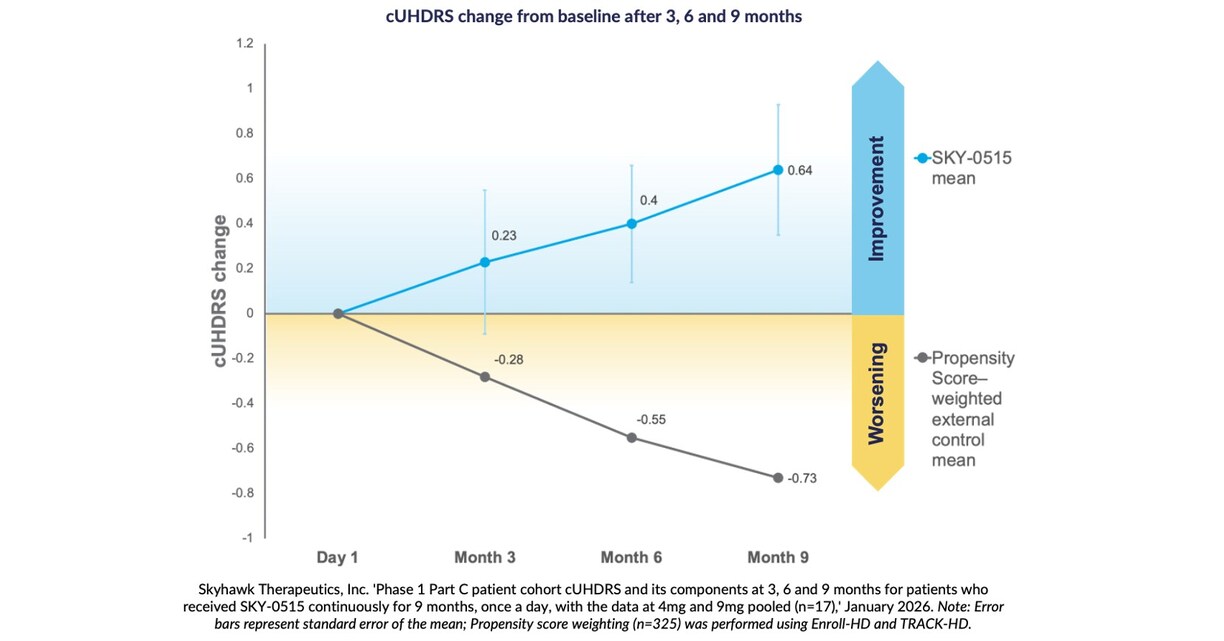
Deväťmesačné zistenia ukazujú priemerné zlepšenie v zjednotenej stupnici hodnotenia Huntingtonovej choroby (Composite Unified Huntington’s Disease Rating Scale, cUHDRS) oproti východiskovej hodnote o +0,64 bodu, v porovnaní s prirodzeným očakávaným zhoršením cUHDRS u symptomatických pacientov o -0,73 bodu počas deviatich mesiacov na základe váženia skóre propensity.
Spoločnosť Skyhawk tiež oznamuje, že klinické skúšanie fázy 2/3 FALCON-HD lieku SKY-0515 sa rozšírilo po celom svete. Spoločnosť Skyhawk už podala dávku viac ako 90 pacientom.
BOSTON, 28. januára 2026 /PRNewswire/ — Spoločnosť Skyhawk Therapeutics, Inc., biotechnologická spoločnosť v klinickom štádiu, ktorá vyvíja nové terapie s malými molekulami na moduláciu kritických cieľov RNA, dnes oznamuje pozitívne výsledky deväťmesačnej predbežnej analýzy skúmanej liečby Huntingtonovej choroby (HD) s liekom SKY-0515. Liečba liekom SKY-0515 vedie k dávkovo závislému zníženiu hladiny proteínu mHTT v krvi o 62 % pri dávke 9 mg a k dávkovo závislému zníženiu hladiny mRNA proteínu PMS1 o 26 %. Proteín PMS1 je kľúčovým faktorom expanzie opakovaní somatického CAG a patológie HD. Liek SKY-0515 tiež preukázal vynikajúci vplyv na centrálny nervový systém a bol vo všeobecnosti bezpečný a dobre tolerovaný. Po troch, šiestich a deviatich mesiacoch pacienti užívajúci liek SKY-0515 v kohorte pacientov časti C klinického skúšania fázy 1 s liekom SKY-0515 vykazujú priemerné zlepšenie na zjednotenej stupnici hodnotenia Huntingtonovej choroby (cUHDRS) oproti východiskovému stavu. V súhrnnej analýze je toto zlepšenie po deviatich mesiacoch o +0,64 bodu v porovnaní s očakávaným zhoršením po deviatich mesiacoch cUHDRS u symptomatických pacientov o -0,73 bodu, na základe váženia skóre propensity pomocou platformy Enroll-HD a skúšania TRACK-HD. „Veľmi ma povzbudzujú tieto údaje o bezpečnosti a skorej účinnosti zo skúšania fázy 1 časti C lieku SKY-0515 u pacientov, ktoré ukazujú odchýlku v cUHDRS od očakávaného zhoršenia prirodzeného priebehu vo vopred špecifikovaných analýzach po troch, šiestich a deviatich mesiacoch,” povedal Ed Wild, profesor neurológie na University College London. „Liek SKY-0515 naďalej znižuje hladinu mHTT proteínu v najväčšej miere, akú doteraz preukázala akákoľvek testovaná liečba u pacientov, pričom klinické údaje a údaje o biomarkeroch ukazujú, že liek je dobre tolerovaný vo všetkých testovaných dávkach. Schopnosť lieku SKY-0515 znižovať proteín mHTT aj PMS1 ponúka účinnú kombináciu na liečbu Huntingtonovej choroby prostredníctvom dvoch jej základných patogénnych mechanizmov. Tieto výsledky otvoreného klinického skúšania, ktoré majú byť validované v prebiehajúcom placebom kontrolovanom skúšaní FALCON-HD, vyvolávajú očakávanie významného vplyvu na ľudí žijúcich s HD na celom svete – pre ktorých bude skutočne transformačná perorálne podávaná liečba, ako napríklad v podobe lieku SKY-0515, ktorý znižuje hladinu huntingtínu.” „Naším cieľom v našom klinickom skúšaní fázy 1 bolo stanoviť bezpečnosť a aktivitu biomarkerov,” povedal Sergej Pauškin, vedúci výskumu a vývoja v spoločnosti Skyhawk Therapeutics, „a pokračujúca silná odpoveď biomarkerov na liek SKY-0515 v našej deväťmesačnej priebežnej analýze údajov – a zlepšenie potenciálneho sledovaného parametra, cUHDRS, v porovnaní so zhoršením skóre cUHDRS v údajoch o prirodzenom priebehu u pacientov – podčiarkuje potenciál lieku SKY-0515 ako najlepšej liečby modifikujúcej ochorenie pri HD vo svojej triede. Tieto predbežné údaje predstavujú dôležitý míľnik pre liek SKY-0515 a zdôrazňujú silu platformy Skyhawk pri poskytovaní prvotriednych malých molekúl v prípade ničivých chorôb bez schválených terapií modifikujúcich ochorenie.” Huntingtonova choroba je zriedkavé, dedičné a nakoniec smrteľné neurodegeneratívne ochorenie, ktoré postihuje viac ako 40 000 symptomatických pacientov v Spojených štátoch a odhaduje sa, že na celom svete ňou trpia státisíce pacientov. V súčasnosti neexistujú žiadne schválené liečebné postupy, ktoré by spomalili alebo zastavili progresiu ochorenia. Liek SKY-0515 je perorálne podávaný, experimentálny nízkomolekulárny RNA modulátor vyvinutý prostredníctvom novej RNA-modulačnej platformy spoločnosti SKYSTAR®. Liek SKY-0515 terapeuticky redukuje proteín HTT ako aj proteín PMS1. Proteín PMS1 je ďalším kľúčovým faktorom expanzie opakovaní somatického CAG a patológie HD a mal by dopĺňať výhody redukcie mutantného HTT. Spoločnosť Skyhawk dnes tiež oznámila, že jej klinické skúšanie lieku SKY-0515 fázy 2/3 FALCON-HD, ktoré prebieha na dvanástich miestach v Austrálii a na Novom Zélande, sa rozšírilo do celého sveta. Spoločnosť Skyhawk už podala liek SKY-0515 viac ako 90 pacientom. SKY-0515 je prvý liek od spoločnosti Skyhawk, ktorý je v klinických skúšaniach. Spoločnosť Skyhawk očakáva, že do konca roka 2027 uvedie do klinického prostredia ďalšie lieky s malými molekulami na liečbu zriedkavých neurologických ochorení, pre ktoré ešte neboli schválené žiadne chorobu modifikujúce terapie. O klinickom skúšaní fázy 1 lieku SKY-0515Klinické skúšanie fázy 1 lieku SKY-0515 je prvé skúšanie na ľuďoch, ktoré je navrhnuté na vyhodnotenie bezpečnosti, znášanlivosti, farmakokinetiky a farmakodynamiky lieku SKY-0515 u zdravých dobrovoľníkov a jedincov s Huntingtonovou chorobou (HD) v ranom štádiu. Klinické skúšanie je rozdelené na tri časti. V častiach A a B sa hodnotil liek SKY-0515 u zdravých dobrovoľníkov. Časť C je dvojito zaslepené placebom kontrolované paralelné skúšanie s dvoma úrovňami dávok lieku SKY-0515 a placeba u jedincov s HD v ranom štádiu (HD-ISS štádium 1, 2 alebo mierne štádium 3) počas 84 dní, po ktorých nasledovalo 12-mesačné predĺženie aktívnej liečby, kde všetci účastníci dostali buď nízku, alebo vysokú dávku lieku SKY-0515 v zaslepenej fáze skúšania. Ciele skúšania zahŕňajú vyhodnotenie mutantného HTT proteínu a mRNA proteínu PMS1. Prví pacienti dostali dávku lieku SKY-0515 v časti C skúšania v januári 2025. Nábor do fázy 1C klinického skúšania lieku SKY-0515 je teraz ukončený. O klinickom skúšaní FALCON-HD lieku SKY-0515 fázy 2/3
FALCON-HD (NCT06873334) je randomizované, dvojito zaslepené, placebom kontrolované skúšanie fázy 2/3 s rôznym dávkovaním, ktoré hodnotí farmakodynamiku, bezpečnosť a účinnosť lieku SKY-0515 u 120 účastníkov s HD v 2. štádiu a rannom 3. štádiu na 12 miestach v Austrálii a na Novom Zélande a u 400 účastníkov s HD v 2. štádiu a rannom 3. štádiu na viac ako 40 miestach po celom svete. Vhodní pacienti budú dostávať raz denne perorálnu dávku lieku SKY-0515 v jednej z troch úrovní dávkovania alebo placebo počas obdobia liečby najmenej 12 mesiacov. Cieľom štúdie je posúdiť potenciál lieku SKY-0515 modulovať zostrih RNA a redukovať proteíny mHTT a PMS1, ktoré sú zapojené do patológie Huntingtonovej choroby. Ďalšie informácie o klinickom skúšaní FALCON-HD vrátane zúčastnených pracovísk a kritérií oprávnenosti nájdete na webových stránkach ClinicalTrials.gov a www.FALCON-HD.com. O spoločnosti Skyhawk Therapeutics
Skyhawk Therapeutics je biotechnologická spoločnosť v klinickom štádiu, ktorá využíva svoju vlastnú platformu SKYSTAR® na objavovanie a vývoj nízkomolekulárnych RNA modulačných terapií pre najťažšie liečiteľné choroby na svete. Viac informácií nájdete na stránke www.skyhawktx.com. Kontakt na Skyhawk
Maura McCarthyová
vedúca oddelenia rozvoja spoločnosti
[email protected] Fotografia – https://mma.prnewswire.com/media/2870056/Skyhawk_Therapeutics_9_MONTH_DATA_Graph.jpg
Logo – https://mma.prnewswire.com/media/710814/Skyhawk_Therapeutics_Logo.jpg

Source link













Leave a Reply